¿Cuál es la diferencia entre la cinética química y el equilibrio químico?
El Diferencia clave entre la cinética química y el equilibrio químico es que la cinética química trata con las velocidades de reacción, mientras que el equilibrio químico se ocupa de la naturaleza inmutable de las concentraciones de reactivos y productos a lo largo del tiempo.
La cinética química es la rama de la química física relacionada con la comprensión de las tasas de reacciones químicas. El equilibrio químico es la fase donde se producen tanto los reactivos como los productos en concentraciones que no tienen más intención de cambiar con el tiempo.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la cinética química?
3. ¿Qué es el equilibrio químico?
4. Cinética química vs equilibrio químico en forma tabular
5. Resumen - Cinética química vs equilibrio químico
¿Qué es la cinética química??
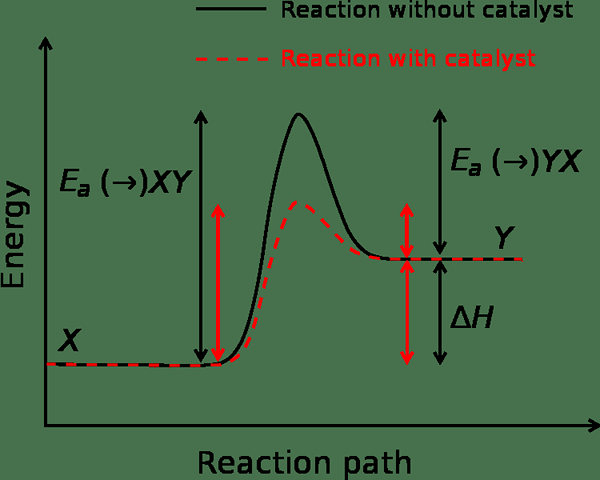
La cinética química puede describirse como la rama de la química física relacionada con la comprensión de las tasas de reacciones químicas. Este término se discute en contraste con la termodinámica. El término cinética química incluye la investigación de condiciones experimentales que pueden influir en la velocidad de una reacción química particular y información sobre el mecanismo de la reacción, así como sus posibles estados de transición. Además, este fenómeno trata con modelos matemáticos que describen las características de una reacción.

Los principales factores que afectan la cinética química son la naturaleza de los reactivos, el estado físico, el área superficial del estado sólido, la concentración, la temperatura, la catálisis, la presión, la absorción de la luz, etc.
Existen diferentes métodos para determinar la velocidad de reacción de una reacción química particular. Aquí, necesitamos medir la concentración de reactivos o productos que cambian con el tiempo. mi.gramo. Podemos medir la concentración de un reactante por espectrofotometría cuando se relacionan con una longitud de onda en la que ningún otro reactivo o producto de ese sistema puede absorber la luz.
¿Qué es el equilibrio químico??
El equilibrio químico es la fase donde se producen tanto los reactivos como los productos en concentraciones que no tienen más intención de cambiar con el tiempo. Hay reacciones químicas reversibles, así como reacciones irreversibles. Una reacción química implica reactivos para convertirse en productos. A veces, los reactivos se generan a partir de los productos. Estas son reacciones reversibles. Pero a veces, los reactivos se consumen por completo a lo largo de la reacción y no se hacen de nuevo. Estas son reacciones irreversibles. En una reacción reversible, cuando los reactivos se están convirtiendo a productos, lo llamamos una reacción hacia adelante, y cuando los productos se están convirtiendo a reactivos, es una reacción hacia atrás.
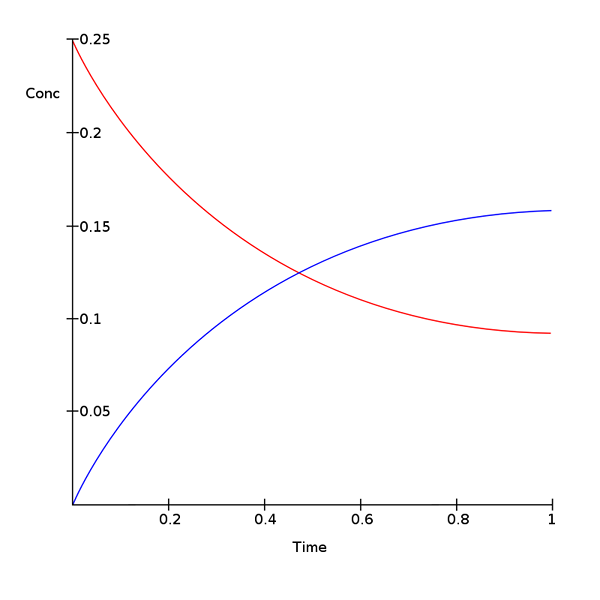
Si las velocidades de reacción hacia adelante y hacia atrás son iguales, entonces la reacción está en equilibrio. Por lo tanto, durante algún tiempo, la cantidad de reactivos y productos no cambia. Las reacciones reversibles siempre tienden a llegar al equilibrio y mantienen ese equilibrio. Cuando el sistema está en equilibrio, la cantidad de productos y los reactivos no son necesariamente iguales. Puede haber una mayor cantidad de reactivos que los productos o viceversa. El único requisito en una ecuación de equilibrio es el mantenimiento de una cantidad constante de ambos con el tiempo. Para una reacción en equilibrio, podemos definir una constante de equilibrio como: es igual a la relación entre la concentración de productos y la concentración de reacciones.
¿Cuál es la diferencia entre la cinética química y el equilibrio químico??
Los términos cinéticos químicos y el equilibrio químico son muy importantes en la química. Estos se aplican en casi todas las ocasiones en la naturaleza. La diferencia clave entre la cinética química y el equilibrio químico es que la cinética química se ocupa de las velocidades de reacción, mientras que el equilibrio químico se ocupa de la naturaleza inmutable de las concentraciones de reactivos y productos a lo largo del tiempo.
La siguiente infografía presenta las diferencias entre la cinética química y el equilibrio químico en forma tabular para la comparación de lado a lado.
Resumen -Cinética química vs equilibrio químico
La cinética química es la rama de la química física relacionada con la comprensión de las tasas de reacciones químicas. El equilibrio químico es la fase donde se producen tanto los reactivos como los productos en concentraciones que no tienen más intención de cambiar con el tiempo. La diferencia clave entre la cinética química y el equilibrio químico es que la cinética química se ocupa de las velocidades de reacción, mientras que el equilibrio químico se ocupa de la naturaleza inmutable de las concentraciones de reactivos y productos a lo largo del tiempo.
Referencia:
1. "Equilibrio químico." Enciclopía Britannica, Encyclopædia Britannica, Inc.
Imagen de cortesía:
1. "Energía de activación" (uso gratuito con derechos de autor) a través de Commons Wikimedia
2. "Equilibrio químico" por Fintelia - Trabajo propio (CC BY -SA 3.0) a través de Commons Wikimedia


