¿Cuál es la diferencia entre epoxidación y oxidación?
El Diferencia clave entre epoxidación y oxidación es que la epoxidación se refiere a la conversión de un grupo de carbono de doble enlace en un grupo de epóxido, mientras que la oxidación se refiere a la combinación de oxígeno con una sustancia.
Epoxidación y oxidación son términos comunes en las reacciones de síntesis orgánica. La epoxidación se puede describir como una forma especial de oxidación que específicamente proporciona un compuesto de óxido cíclico/ compuesto de epóxido.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la epoxidación?
3. ¿Qué es la oxidación?
4. Similitudes - epoxidación y oxidación
5. Epoxidación frente a oxidación en forma tabular
6. Resumen -Epoxidación vs oxidación
¿Qué es la epoxidación??
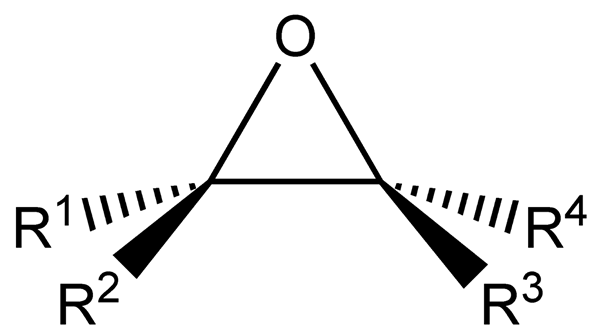
La epoxidación es el proceso químico que puede convertir un enlace químico C-C en un enlace de epóxido. Un epóxido es un éter cíclico que tiene ambos átomos de carbono de un doble enlace unido al mismo átomo de oxígeno. Estos compuestos también se llaman oxiranos.

Figura 01: Estructura general de un epóxido
Podemos crear un epóxido a través de la reacción entre los peráculos y los átomos de carbono de doble enlace. En los peracidos, hay un enlace de oxígeno-oxígeno que no solo es débil sino también un enlace polarizado. Por lo tanto, el grupo aciloxi en este compuesto tiene una carga negativa, y el grupo hidroxilo tiene una carga positiva. Sin embargo, es poco probable que se forme un intermedio dipolar, por lo que los científicos creen que esta reacción ocurre en un solo paso a través de una transición que incorpora todos los eventos de unión química y rompiendo el enlace al mismo tiempo.
¿Qué es la oxidación??
La oxidación es el proceso de aumentar el número de oxidación de especies químicas. Sin embargo, hay tres definiciones distintas para este término; La adición de oxígeno, eliminación de hidrógeno o pérdida de electrones significa oxidación. Pero todas estas definiciones tienen excepciones en diferentes ocasiones. Por lo tanto, usamos la definición anterior como definición general para todas las ocasiones.
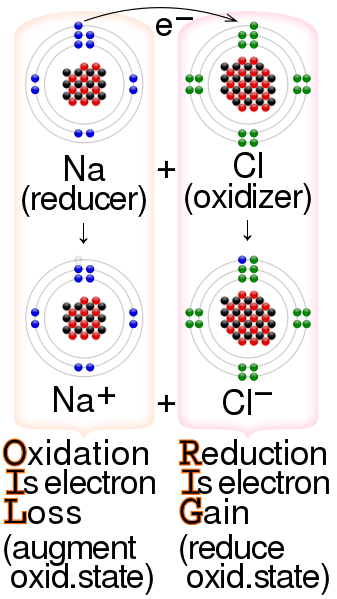
Figura 02: Reacción de reducción-oxidación
La oxidación es un tipo de reacción redox. Una reacción redox esencialmente tiene dos reacciones paralelas: reacciones de oxidación y reacciones de reducción. Estas reacciones siempre implican la transferencia de electrones entre dos especies químicas. Además, las especies químicas que sufre oxidación siempre liberarán electrones, mientras que las especies químicas que sufre reducción siempre obtendrán esos electrones. Por lo tanto, liberar electrones hace más protones que no tienen electrones para neutralizar su carga. Por lo tanto, la eliminación de electrones aumentará el número de oxidación de las especies químicas.
¿Cuáles son las similitudes entre epoxidación y oxidación??
- Epoxidación y oxidación son tipos de reacciones de oxidación que implican la adición de átomos de oxígeno a los compuestos orgánicos.
- Ambas reacciones son importantes en las reacciones de síntesis orgánica.
- Estas reacciones dan tipos de compuestos de óxido como producto final.
¿Cuál es la diferencia entre epoxidación y oxidación??
Epoxidación y oxidación son términos comunes en las reacciones de síntesis orgánica. La diferencia clave entre la epoxidación y la oxidación es que la epoxidación se refiere a la conversión de un grupo de carbono de doble enlace en un grupo de epóxido, mientras que la oxidación se refiere a la combinación de oxígeno con una sustancia. Por lo tanto, la reacción de epoxidación proporciona un epóxido como producto final de la reacción, que es un grupo cíclico que involucra un átomo de oxígeno y dos átomos de carbono. Por otro lado, la oxidación proporciona un compuesto de óxido como producto final, que tiene un enlace de carbono a oxígeno que no es cíclico.
La siguiente infografía presenta la diferencia entre epoxidación y oxidación en forma tabular.
Resumen -Epoxidación vs oxidación
Epoxidación y oxidación son términos comunes en las reacciones de síntesis orgánica. La diferencia clave entre la epoxidación y la oxidación es que la epoxidación se refiere a la conversión de un grupo de carbono de doble enlace en un grupo de epóxido, mientras que la oxidación se refiere a la combinación de oxígeno con una sustancia.
Referencia:
1. "Epoxidación." Bibliotecas de química, Libretexts, 13 de septiembre. 2020.
Imagen de cortesía:
1. "Epóxido genérico" de Tomas Bindahl - Trabajo propio (dominio público) a través de Commons Wikimedia
2. "Ejemplo redox" de CMGLEE - Trabajo propio (CC By -SA 4.0) a través de Commons Wikimedia