¿Cuál es la diferencia entre conductancia equivalente y conductancia molar?
El Diferencia clave entre conductancia equivalente y conductancia molar Es que la conductancia equivalente es la conductancia de un electrolito que se divide por el número de equivalentes del electrolito por unidad de volumen, mientras que la conductancia molar es la conductancia de un electrolito dividido por el número de moles del electrolito.
La conductancia molar es la conductancia de todos los iones proporcionados por un lunar de un electrolito presente en un volumen definido de la solución. La conductancia equivalente es la conductancia de un volumen de una solución que consiste en un peso equivalente de sustancia disuelta cuando se coloca entre dos electrodos paralelos.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es una conductancia equivalente?
3. ¿Qué es la conductancia molar?
4. Conductancia equivalente frente a conductancia en forma tabular
5. Resumen -conductancia equivalente vs conductancia molar
¿Qué es una conductancia equivalente??
La conductancia equivalente es la conductancia de un volumen de una solución que consiste en un peso equivalente de sustancia disuelta cuando se coloca entre dos electrodos paralelos. Los electrodos se colocan con una distancia de 1 cm entre ellos. Es lo suficientemente grande como para contener la solución entre ellos. Se puede describir como la conductancia neta de cada ion que se produce a partir de 1 gramo equivalente de una sustancia particular. El cálculo para este parámetro se realiza de la siguiente manera:
λ = kV
En esta ecuación, λ es una conductancia equivalente, k es una constante y v es el volumen en mililitros administrados para 1 gramo equivalente del electrolito que estamos utilizando para esta determinación.

¿Qué es la conductancia molar??
La conductancia molar es la conductancia de todos los iones proporcionados por un lunar de un electrolito presente en un volumen definido de la solución. El término conductividad molar se refiere a la propiedad de tener una conductancia molar.
La conductividad molar es la conductividad de una solución electrolítica medida por unidad de concentración molar de la solución. Podemos determinar esto como la conductividad de la solución electrolítica dividida por la concentración molar del electrolito. Por lo tanto, podemos dar la conductividad molar en la siguiente ecuación:
Conductividad molar = k/c
k es la conductividad medida de la solución electrolítica, y C es la concentración de la solución electrolítica.
Al considerar la medición de la conductividad molar, la unidad SI para la medición de esta propiedad son los medidores de Siemens al cuadrado por lunar. Entonces la unidad se da como s m2 moles-1. Sin embargo, la mayoría de las veces, la unidad para esta propiedad es S CM2 moles-1.
¿Cuál es la diferencia entre conductancia equivalente y conductancia molar??
La conductancia molar es la conductancia de todos los iones proporcionados por un lunar de un electrolito presente en un volumen definido de la solución. La conductancia equivalente, por otro lado, es la conductancia de un volumen de una solución que consiste en un peso equivalente de sustancia disuelta cuando se coloca entre dos electrodos paralelos. La diferencia clave entre la conductancia equivalente y la conductancia molar es que la conductancia equivalente es la conductancia de un electrolito que se divide por el número de equivalentes del electrolito por unidad de volumen, mientras que la conductancia molar es la conductancia de un electrolito dividido por el número de moles de moles de moles el electrolito.
La siguiente infografía presenta las diferencias entre la conductancia equivalente y la conductancia molar en forma tabular para la comparación de lado a lado.
Resumen -conductancia equivalente vs conductancia molar
La conductancia equivalente y la conductancia molar son dos tipos de conductividades. La diferencia clave entre la conductancia equivalente y la conductancia molar es que la conductancia equivalente es la conductancia de un electrolito que se divide por el número de equivalentes del electrolito por unidad de volumen, mientras que la conductancia molar es la conductancia de un electrolito dividido por el número de moles de moles de moles el electrolito.
Referencia:
1. "Conductividad molar." Una descripción general | Temas de ciencias.
Imagen de cortesía:
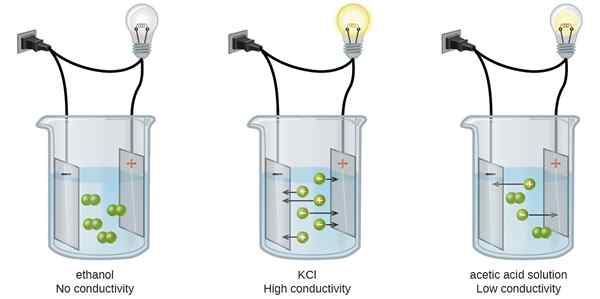
1. "Conductividad (Electrolítica) 2" de Karishma50 - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia


