¿Cuál es la diferencia entre la primera ley y la segunda ley de la termodinámica?
El diferencia clave entre la primera ley y la segunda ley de la termodinámica es que la primera ley de la termodinámica establece que la energía no puede ser creada o destruida, y la cantidad total de la energía en el universo permanece igual, mientras que la segunda ley de la termodinámica describe la naturaleza de la energía.
La termodinámica se refiere a la rama de la ciencia física que trata las relaciones entre el calor y otras formas de energía, como la energía mecánica, eléctrica o química.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Cuál es la primera ley de la termodinámica?
3. ¿Cuál es la segunda ley de la termodinámica?
4. Primera Ley vs SEGUNDA LEY DE TERMODYNICS en forma tabular
5. Resumen -Primera ley vs SEGUNDA LEY DE TERMODYNICS
¿Cuál es la primera ley de la termodinámica??
La primera ley de la termodinámica describe que la energía interna de un sistema es la diferencia entre la energía que absorbe de los alrededores y el trabajo realizado por el sistema en el entorno. Esta es una versión de la Ley de Conservación de Energía que se adapta a los procesos termodinámicos. Distinga tres tipos de transferencia de energía: calor, trabajo termodinámico y energía interna.
Podemos dar la primera ley de la termodinámica sin transferencia de masa de la siguiente manera:
ΔU = Q - W
En esta expresión, ΔU se refiere al cambio en la energía interna de un sistema cerrado, mientras que Q denota la cantidad de energía suministrada al sistema como calor, mientras que W es la cantidad de trabajo termodinámico realizado por el sistema en el entorno.

Además, la primera ley de la termodinámica con necesidades de transferencia de masa implica más condiciones; Con la debida cuenta de los estados de referencia correspondientes del sistema, cuando dos sistemas están separados solo por una pared impermeable, se combinan en un nuevo sistema mediante la operación termodinámica de eliminación de esta pared, lo que conduce a la siguiente expresión:
U0 = U1 + U2
Donde U0 es la energía interna del sistema combinado, U1 y U2 son las energías internas de los sistemas correspondientes.
¿Cuál es la segunda ley de la termodinámica??
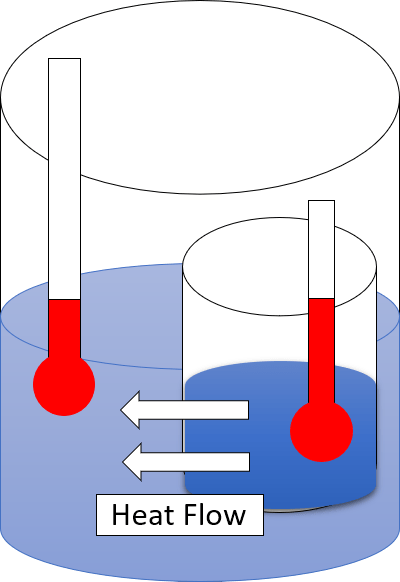
La segunda ley de la termodinámica describe que el calor no puede fluir de una ubicación más fría a un área más caliente espontáneamente. Es la ley física de la termodinámica la que describe el calor y la pérdida en la conversión. La forma más sencilla de expresar la segunda ley de la termodinámica es "no toda la energía térmica puede convertirse en trabajo."
Según las otras versiones de esta ley, el concepto de entropía se establece como una propiedad física de un sistema termodinámico. Podemos formular la segunda ley de la termodinámica a través de la observación "La entropía de los sistemas aislados que quedan a la evolución espontánea no puede disminuir porque siempre llegan a un estado de equilibrio termodinámico (esto sucede donde la entropía es más alta en la energía interna dada).
¿Cuál es la diferencia entre la primera ley y la segunda ley de la termodinámica??
La termodinámica se refiere a la rama de la ciencia física que trata las relaciones entre el calor y otras formas de energía, como la energía mecánica, eléctrica o química. La diferencia clave entre la primera ley y la segunda ley de la termodinámica es que la primera ley de la termodinámica afirma que la energía no puede ser creada o destruida y la cantidad total de energía en el universo permanece igual, mientras que la segunda ley de la termodinámica describe que el El calor no puede fluir de una ubicación más fría a un área más caliente espontáneamente.
La siguiente infografía presenta las diferencias entre la primera ley y la segunda ley de la termodinámica en forma tabular para la comparación de lado a lado.
Resumen -Primera ley vs SEGUNDA LEY DE TERMODYNICS
La primera ley de la termodinámica describe que la energía interna de un sistema es la diferencia entre la energía que absorbe de los alrededores y el trabajo realizado por el sistema en el entorno. La segunda ley de la termodinámica describe que el calor no puede fluir de una ubicación más fría a un área más caliente espontáneamente. Entonces, esta es la diferencia clave entre la primera ley y la segunda ley de la termodinámica.
Referencia:
1. "Segunda ley de la termodinámica." NASA.
Imagen de cortesía:
1. "Flujo de calor caliente a frío" de Blyumj - Trabajo propio (CC By -SA 4.0) a través de Commons Wikimedia


