¿Cuál es la diferencia entre la ley de Gay-Lussac y la ley de Avogadro?
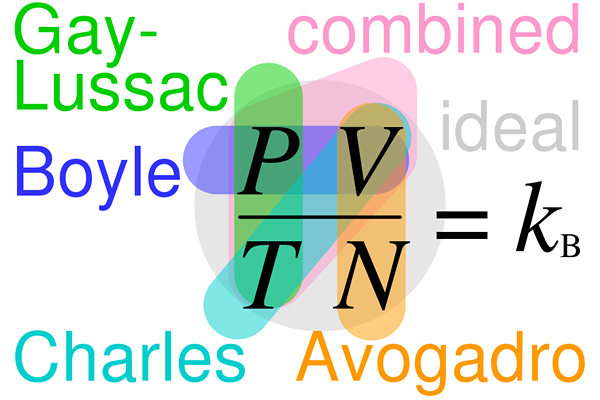
El Diferencia clave entre la ley de Gay-Lussac y la ley de Avogadro Es que la ley de Gay-Lussac indica que el volumen de un gas es directamente proporcional a la temperatura del gas, mientras que la ley de Avogadro establece que el volumen de un gas es directamente proporcional al número de moléculas en el gas.
La ley de Gay-Lussac describe la variable de la presión de una masa particular de un gas directamente con la temperatura absoluta del gas con volumen constante. La ley de Avogadro es una ley de gas experimental que establece que el volumen de un gas está relacionado con la cantidad de gas de sustancia presente en una muestra dada.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la ley de Gay-Lussac?
3. ¿Cuál es la ley de Avogadro?
4. Ley de Gay-Lussac vs Avogadro's Ley en forma tabular
5. Resumen -Ley de Gay -Lussac vs Avogadro's Ley
¿Qué es la ley de Gay-Lussac??
La ley de Gay-Lussac describe la variable de la presión de una masa particular de un gas directamente con la temperatura absoluta del gas con volumen constante. A veces se llama la ley de Amonton. Podemos dar una expresión matemática para esta ley de la siguiente manera:
P/T = K
En esta ecuación, P se refiere a la presión, T se refiere a la temperatura absoluta, y K es una constante. Podemos decir que este es un caso especial de ley de gas ideal.
Un derivado de esta ley es la ley de temperatura de presión, que describe la relación entre la presión y la temperatura de una cierta masa de un gas a un volumen constante.
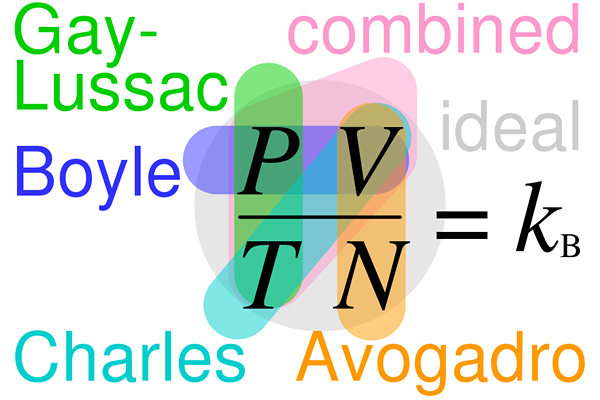
Según la ley de combinar volúmenes, los gases reaccionan entre sí por medio de volumen, y reaccionan en una relación de número entero a condiciones de temperatura y presión constantes. En otras palabras, la relación entre los volúmenes de los gases reactivos y los productos gaseosos se puede dar en números enteros simples. Gay Lussac fue uno de los primeros científicos en descubrir esta relación, lo que condujo a la derivación de la ley de Avogadro.
¿Cuál es la ley de Avogadro??
La ley de Avogadro es una ley de gas experimental que establece que el volumen de un gas está relacionado con la cantidad de gas de sustancia presente en una muestra dada. También se llama Hipótesis de Avogadro o el principio de Avogadro. Esta es una forma específica de ley de gas ideal. Esta ley lleva el nombre de Amedeo Avogadro en 1812.
Según las descripciones modernas, la ley de Avogadro establece que los volúmenes iguales de todos los gases que están en una temperatura y una condición de presión tienen el mismo número de moléculas. Por ejemplo, los volúmenes iguales de gas de hidrógeno y gas nitrógeno consisten en un número igual de átomos cuando estos dos gases están en la misma temperatura y presión. Prácticamente, los gases reales muestran pequeñas desviaciones del comportamiento de gas ideal donde la ley es solo aproximadamente precisa. Sin embargo, sigue siendo una aproximación importante para los científicos. Matemáticamente, la ley es la siguiente:
V/N = K
Donde v es el volumen del gas, n es la cantidad de sustancia del gas en la muestra, y k es un valor constante dado para una temperatura y presión particulares.
Diferencia entre la ley de Gay-Lussac y la ley de Avogadro
La ley de Gay-Lussac y la ley de Avogadro son dos leyes importantes de gas. La diferencia clave entre la ley de Gay-Lussac y la ley de Avogadro es que la ley de Gay-Lussac indica que el volumen de un gas es directamente proporcional a la temperatura del gas, mientras que la ley de Avogadro establece que el volumen de un gas es directamente proporcional al número de moléculas en el gas.
La siguiente tabla resume la diferencia entre la ley de Gay-Lussac y la ley de Avogadro.
Resumen -Ley de Gay -Lussac vs Avogadro's Ley
La ley de Gay-Lussac y la ley de Avogadro son dos leyes importantes de gas. La diferencia clave entre la ley de Gay-Lussac y la ley de Avogadro es que la ley de Gay-Lussac indica que el volumen de un gas es directamente proporcional a la temperatura del gas, mientras que la ley de Avogadro establece que el volumen de un gas es directamente proporcional al número de moléculas en el gas.
Referencia:
1. "Ley de Gay -Lussac - declaración, fórmula, explicación detallada." Byjus, 25 de mar. 2021.
Imagen de cortesía:
1. "Relaciones ideales de la ley de gas" por CMGLEE - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia


