¿Cuál es la diferencia entre los orbitales hibridados y noridiados?
El Diferencia clave entre los orbitales hibridados y nobriados es que los orbitales hibridados son híbridos o mezclas de orbitales atómicos, mientras que los orbitales nobriados son orbitales atómicos regulares que no se mezclan con otros orbitales atómicos.
La comprensión de los orbitales hibridados y nobriados es muy importante para estudiar y predecir estructuras químicas de compuestos químicos. Los orbitales hibridados son combinaciones de orbitales nobriados.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la hibridación orbital?
3. ¿Qué son los orbitales hibridados?
4. ¿Qué son los orbitales noridiados?
5. Orbitales hibridados versus nobridados en forma tabular
6. Resumen - Hibridados frente a orbitales nobriados
¿Qué es la hibridación orbital??
La hibridación orbital es un concepto muy importante en química. Es el concepto de mezclar orbitales atómicos y formar nuevos orbitales híbridos el que son adecuados para el emparejamiento de electrones en la formación de enlaces químicos de acuerdo con la teoría del enlace de valencia. Por ejemplo, un átomo de carbono que puede formar cuatro enlaces individuales contiene cuatro electrones de carcasa de valencia en cuatro orbitales híbridos que se forman a partir de la hibridación de un orbital atómico "S" con tres orbitales atómicos P.
Los orbitales atómicos son representaciones modelo del comportamiento de los electrones dentro de las moléculas. Una hibridación simple es una aproximación que se realiza en base a orbitales atómicos que son similares a los obtenidos para el átomo de hidrógeno. Es el único átomo que podemos resolver la ecuación de Schrodinger. Al considerar átomos pesados como el carbono y el nitrógeno, los orbitales atómicos usan orbitales atómicos 2S y 2P que son similares a los orbitales de estado excitado para hidrógeno.
¿Qué son los orbitales hibridados??
Los orbitales hibridados son orbitales atómicos mixtos o combinados involucrados en la unión química. Son orbitales atómicos híbridos mixtos que son útiles en la explicación de la geometría molecular y las propiedades de unión atómica. Estos están simétricamente dispuestos en el espacio. Típicamente, los orbitales hibridados se forman a partir de la mezcla de orbitales atómicos de energías comparables.
Los orbitales híbridos se pueden suponer como mezclas de orbitales atómicos. Estos se superponen el uno al otro en varias proporciones. Por ejemplo, en el metano, hay un enlace de hidrógeno de carbono en el que el orbital híbrido del átomo de carbono tiene 25% S de carácter y 75% de carácter P. Por lo tanto, se describe como un orbital híbrido SP3. Existen diferentes tipos de hibridizaciones, incluidas SP, SP2 y SP3.

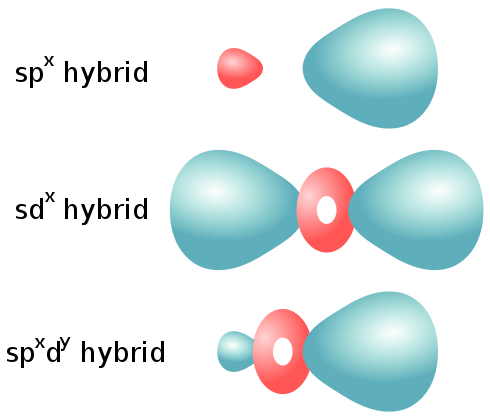
Forma de los orbitales SP a partir de la hibridación de uno sy un orbital atómico P. Este tipo de orbitales hibridados se puede encontrar en alquinos que tienen enlaces triples. Esta combinación da como resultado dos orbitales hibridados SP y dos orbitales atómicos P restantes.
En general, la hibridación es útil para explicar la forma molecular. Esto se debe a que el ángulo entre enlaces es aproximadamente igual al ángulo entre los orbitales híbridos.
¿Qué son los orbitales noridiados??
Los orbitales nobriados son orbitales atómicos regulares que no se mezclan con otros orbitales atómicos. Los orbitales atómicos de P nobriados se utilizan en la formación de enlaces π. Por lo general, dos orbitales atómicos de P no fibridados provenientes de diferentes átomos pueden superponerse de lado a lado, lo que resulta en un par de electrones compartido que ocupa el espacio por encima y por debajo de la línea que une los átomos.
Todos los orbitales nobriados no se encuentran en el estado fundamental del átomo. El uso principal de este tipo de orbital es la formación de enlaces dobles y triples. Por ejemplo, en la hibridación SP3, hay 4 orbitales atómicos hibridados SP3 y sin orbitales nobriados. Por lo tanto, este tipo de hibridación en un átomo puede formar 4 enlaces Sigma. Pero en las hibridizaciones SP2 y SP, quedan uno y dos orbitales de P noridados en el átomo hibridado, respectivamente. Estos orbitales atómicos de P nobriados están involucrados en la formación de enlaces triples y dobles, respectivamente.
¿Cuál es la diferencia entre los orbitales hibridados y noridiados??
La diferencia clave entre los orbitales hibridados y nobriados es que los orbitales hibridados son híbridos o mezclas de orbitales atómicos, mientras que los orbitales nobriados son orbitales atómicos regulares que no se mezclan con otros orbitales atómicos. Mientras que los orbitales hibridados forman enlaces Sigma, los orbitales noridiados forman enlaces PI.
La siguiente infografía presenta las diferencias entre los orbitales hibridados y nobriados en forma tabular para la comparación de lado a lado.
Resumen -Hibridados frente a orbitales nobriados
La diferencia clave entre los orbitales hibridados y nobriados es que los orbitales hibridados son híbridos o mezclas de orbitales atómicos, mientras que los orbitales nobriados son orbitales atómicos regulares que no se mezclan con otros orbitales atómicos.
Referencia:
1. "Orbitales híbridos." Bibliotecas de química, Libretexts, 26 de agosto. 2022.
Imagen de cortesía:
1. "Formas de orbitales híbridos" por Oficial781 - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia


