¿Cuál es la diferencia entre la absorción molar y la absorbancia específica?
El diferencia clave entre la absorción molar y la absorbancia específica es que la absorción molar es la absorbancia de una solución por unidad de longitud y concentración de la ruta, mientras que la absorbancia específica es la absorbancia máxima de una solución al 1% sobre una longitud de ruta de 1 cm medida mediante espectroscopía.
La absorción molar y la absorbancia específica son dos términos importantes en la química que están relacionadas con las propiedades ópticas de las sustancias.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es la absorción molar?
3. ¿Qué es la absorbancia específica?
4. Absorción molar frente a absorbancia específica en forma tabular
5. Resumen -absorción molar frente a absorbancia específica
¿Qué es la absorción molar??
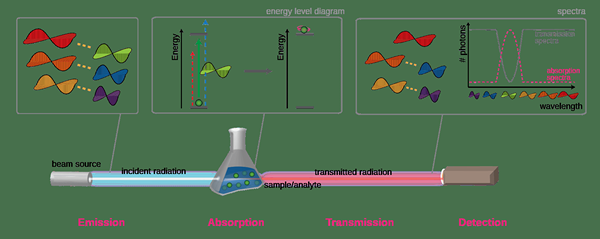
La absorción o la absorción molar es la absorbancia de una solución por unidad de longitud de ruta y concentración. Se origina en la ley de Beer-Lambert. La ley de Beer-Lambert afirma que la absorbancia de las ondas electromagnéticas por una solución es directamente proporcional a la concentración de la solución y la distancia recorrida por el haz de luz.
A α lc
Aquí, A es la absorbancia, L es la longitud del camino (distancia recorrida por el haz de luz), y C es la concentración de la solución. Se utiliza una constante de proporcionalidad para obtener la ecuación para la absorbancia.
La absorbancia es la relación entre la intensidad de la luz antes (i0), y después (i) pasa a través de la solución. Consulte la ecuación a continuación,
A = εbc
Aquí, ε es la absorción molar. También se conoce como el coeficiente de absorción molar. La unidad de la absorción molar se puede obtener de la ecuación anterior, mientras que la unidad de concentración es mol/L (moles por litro), y la unidad de longitud de la ruta es cm (centímetro). La unidad de absorción molar es L mol-1 cm-1 (ya que la absorbancia no tiene unidades). La absorción molar determina cuán fuertemente una solución puede absorber un haz de luz. Además, la absorción molar depende del tipo de analito en la solución.
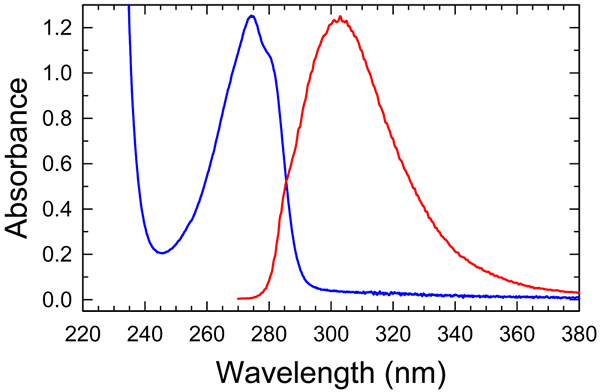
¿Qué es la absorbancia específica??
La absorbancia específica es la absorbancia máxima de una solución al 1% sobre una longitud de ruta de 1 cm medida por espectroscopía. Es denotado por un ... Determinar la absorbancia específica de un fármaco particular proporciona una herramienta importante en la verificación cuantitativa de la concentración de estándares analíticos. La fórmula para la absorbancia específica es la siguiente:
A (1 por ciento, 1 cm) = a/cl
Donde C es la concentración de la sustancia absorbente que se da como un porcentaje W/V, e I es el grosor de la capa de absorción (tomada en cm). Podemos decir que un (1 por ciento, 1 cm) o la absorbancia específica en una solución dada es una propiedad de la sustancia absorbente.

En la espectroscopía, la absorbancia específica es la medición de la absorbancia de la luz en medios mixtos a una longitud de onda específica. Además, la absorbancia de la luz que se mide en una longitud de onda particular puede atribuir a un componente específico o a un grupo de componentes.
¿Cuál es la diferencia entre la absorción molar y la absorbancia específica??
La absorción molar y la absorbancia específica están relacionadas entre sí. La diferencia clave entre la absorción molar y la absorbancia específica es que la absorción molar es la absorbancia de una solución por unidad de longitud y concentración de la ruta, mientras que la absorbancia específica es la absorbancia máxima de una solución al 1% sobre una longitud de ruta de 1 cm medida a través de la espectroscopía de espectroscopio. Mayor la absorción molar, mayor será la absorbancia.
La siguiente tabla resume la diferencia entre la absorción molar y la absorbancia específica.
Resumen -absorción molar frente a absorbancia específica
La diferencia clave entre la absorción molar y la absorbancia específica es que la absorción molar es la absorbancia de una solución por unidad de longitud y concentración de la ruta, mientras que la absorbancia específica es la absorbancia máxima de una solución al 1% sobre una longitud de ruta de 1 cm medida a través de la espectroscopía de espectroscopio. Cuanto mayor es la absorción molar, mayor será la absorbancia.
Referencia:
1. C.H. Semán. "¿Qué es la absorción molar??" Toda la ciencia, 1 de octubre. 2022.
Imagen de cortesía:
1. "Tresina de gripe ABS" de Mark Somoza - Trabajo propio (CC por 2.5) Vía Commons Wikimedia
2. "Descripción general de la espectroscopía" de Jon Chui - Trabajo propio (CC BY -SA 3.0) a través de Commons Wikimedia


