¿Cuál es la diferencia entre solvatación e hidratación?
El Diferencia clave entre solvatación e hidratación es que la solvatación es el proceso de reorganización de las moléculas de solvente y soluto en los complejos de solvatación, mientras que la hidratación se refiere al proceso de agregar una molécula de agua a un compuesto orgánico.
La solvatación y la hidratación son dos procesos importantes en química. La solvatación es la disolución de una sustancia en un solvente particular. Además, la solvatación de un soluto por agua se llama hidratación.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es una solvatación?
3. Que es una hidratación
4. Solvatación frente a hidratación en forma tabular
5. Resumen -Solvación vs Hidratación
Que es la solvatación?
La solvatación puede describirse como la disolución de una sustancia en un solvente particular. Este proceso ocurre debido a la fuerza de atracción entre las moléculas del solvente y las moléculas de soluto. Por lo general, las fuerzas de atracción involucradas en este proceso son enlaces iónicos y atracciones de enlaces de hidrógeno. Estas fuerzas de atracción causan la disolución de un soluto en un solvente.

Las interacciones iónicas-dipolo se pueden encontrar entre compuestos iónicos y solventes polares. Por ejemplo, el agua es un solvente polar. Cuando se agrega cloruro de sodio al agua, las moléculas de agua polar atraen los iones de sodio y los iones de cloruro por separado, lo que hace que los iones de sodio y cloruro se separen. Esto da como resultado la descomposición del compuesto iónico de cloruro de sodio.
Que es la hidratación?
La hidratación puede describirse como la adición de una molécula de agua a un compuesto orgánico. El compuesto orgánico es típicamente un alqueno, que tiene un doble enlace entre dos átomos de carbono. La molécula de agua combina este doble enlace en forma de un grupo hidroxilo (OH-) y un protón (H+). Por lo tanto, la molécula de agua se disocia en sus iones antes de esta adición. El grupo hidroxilo se une a un átomo de carbono del doble enlace, mientras que el protón está unido al otro átomo de carbono.
Dado que implica la ruptura de la unión y la formación de enlaces, la reacción es altamente exotérmica. Eso significa; La reacción libera energía en forma de calor. Es una reacción gradual; En el primer paso, el alqueno actúa como un nucleófilo y ataca el protón de la molécula de agua y se une a través del átomo de carbono menos sustituido. Aquí, la reacción sigue la regla de Markonikov.
El segundo paso incluye la unión del átomo de oxígeno de la molécula de agua al otro átomo de carbono (átomo de carbono altamente sustituido) del doble enlace. En este punto, el átomo de oxígeno de la molécula de agua conlleva una carga positiva porque lleva tres enlaces únicos. Luego viene otra molécula de agua que toma el protón adicional de la molécula de agua unida, dejando el grupo hidroxilo en el átomo de carbono menos sustituido. Por lo tanto, esta reacción conduce a la formación de un alcohol. Sin embargo, los alquinos (unión triple que contiene hidrocarburos) también puede sufrir una reacción de hidratación.
¿Cuál es la diferencia entre solvatación e hidratación??
La solvatación y la hidratación son dos procesos importantes en química orgánica e inorgánica. La diferencia clave entre la solvatación y la hidratación es que la solvatación es el proceso de reorganización de las moléculas de solvente y soluto en complejos de solvatación, mientras que la hidratación se refiere a la adición de una molécula de agua a un compuesto orgánico.
La siguiente tabla resume la diferencia entre solvatación e hidratación.
Resumen -Solvación vs Hidratación
La solvatación puede describirse como la disolución de una sustancia en un solvente particular. La hidratación puede describirse como la adición de una molécula de agua a un compuesto orgánico. Cuando el solvente es agua, la hidratación es similar al proceso de solvatación. La diferencia clave entre la solvatación y la hidratación es que la solvatación es el proceso de reorganización de las moléculas de solvente y soluto en complejos de solvatación, mientras que la hidratación se refiere a la adición de una molécula de agua a un compuesto orgánico.
Referencia:
1. "Solucación." Una descripción general | Temas de ciencias.
Imagen de cortesía:
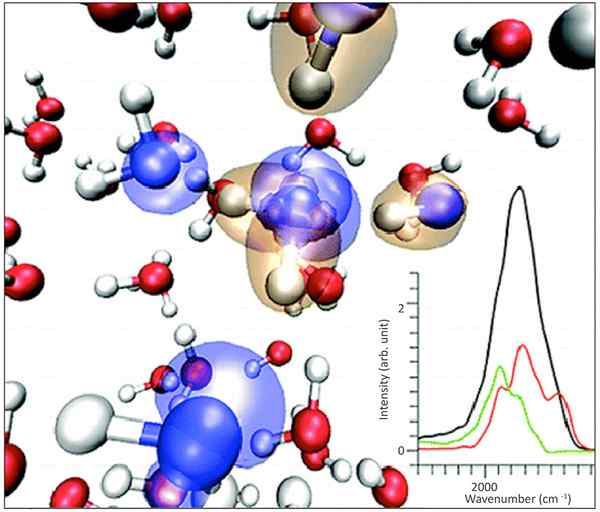
1. "Representación orbital molecular de los estados electrónicos en el primer caparazón de solvatación en el agua" por el Laboratorio Nacional de Argonne (CC BY-NC-SA 2.0) a través de Flickr


