¿Cuál es la diferencia entre el potencial de electrodo estándar y el potencial de reducción estándar?
El Diferencia clave entre el potencial de electrodo estándar y el potencial de reducción estándar es que el potencial de electrodo estándar es la tendencia de un electrodo a perder o ganar electrones, mientras que el potencial de reducción estándar es la tendencia de una especie química a reducirse.
Los términos potencial de electrodo estándar y el potencial de reducción estándar generalmente se usan indistintamente porque es difícil medir el potencial preciso de un electrodo solo en lugar de medir el potencial general. Sin embargo, el potencial de electrodo estándar puede referirse a la oxidación o la reducción, mientras que el potencial de reducción estándar se refiere principalmente a la reducción de la medias reacción.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es el potencial de electrodo estándar?
3. ¿Cuál es el potencial de reducción estándar?
4. Potencial de electrodo estándar frente al potencial de reducción estándar en forma tabular
5. Resumen: potencial de electrodo estándar frente al potencial de reducción estándar
¿Qué es el potencial de electrodo estándar??
El potencial de electrodo estándar puede describirse como la medición del potencial de un equilibrio. En otras palabras, es la diferencia de potencial entre el electrodo y el electrolito llamado como el potencial del electrodo. Mide el poder reductor de cualquier elemento o compuesto. Según el libro de oro IUPAC, el potencial de electrodo estándar es el valor de la EMF estándar (fuerza electromotriz) de una célula donde el hidrógeno molecular bajo presión estándar se oxida a protones solvatados en el electrodo zurdo.
Por lo general, la base de una célula electroquímica es una reacción redox que consta de dos medias reacciones. Estos son la oxidación en el ánodo y la reducción en el cátodo. Por lo tanto, se forma electricidad debido a la diferencia en el potencial eléctrico entre los potenciales individuales de los dos electrodos metálicos con respecto al electrolito.

Simplemente podemos medir el potencial general de una celda. Pero la medición precisa del potencial de electrodo de forma aislada es muy difícil. Este fenómeno varía con la temperatura, la concentración y la presión. El potencial de oxidación de una media reacción puede describirse como el negativo del potencial de reducción en una reacción redox. Por lo tanto, este potencial es suficiente para calcular cualquiera de los potenciales. Esto lleva al uso del potencial de electrodo estándar y el potencial de reducción estándar que se utilizarán indistintamente.
¿Cuál es el potencial de reducción estándar??
El potencial de reducción estándar se puede describir como el potencial en los voltios generado por la medias reacciones de reducción de las reacciones redox en comparación con el electrodo de hidrógeno estándar a 25 grados Celsius, presión de 1 átomo y concentración 1M. En otras palabras, podemos definir este término en relación con un electrodo de hidrógeno estándar. Este electrodo de hidrógeno se asigna como el 0.00 v Estándar potencial. La denotación del potencial de reducción estándar se puede hacer utilizando "E0".
En general, el potencial de reducción estándar se calcula para la media reacción que se produce en el cátodo como la medias reacción de reducción. El potencial de reducción estándar es muy útil en química. A veces, el término potencial de electrodo estándar también se usa indistintamente con este término. La medición de la reducción estándar se realiza utilizando voltios (v). El potencial de reducción estándar nos brinda información sobre la probabilidad de que un elemento o ion se reduzca al obtener electrones.
¿Cuál es la diferencia entre el potencial de electrodo estándar y el potencial de reducción estándar??
La diferencia clave entre el potencial de electrodo estándar y el potencial de reducción estándar es que el potencial de electrodo estándar es la tendencia de un electrodo a perder o ganar electrones, mientras que el potencial de reducción estándar es la tendencia de una especie química dada a reducirse. Sin embargo, estos dos términos se usan indistintamente porque el término potencial de electrodo estándar se puede usar tanto para las medias reacciones de reducción como de oxidación.
La siguiente infografía presenta las diferencias entre el potencial de electrodo estándar y el potencial de reducción estándar en forma tabular para la comparación de lado a lado.
Resumen: potencial de electrodo estándar frente al potencial de reducción estándar
El potencial de electrodo estándar es la medición del potencial de equilibrio, mientras que el potencial de reducción estándar es el potencial en los voltios generados por la medias reacciones de reducción de las reacciones redox. La diferencia clave entre el potencial de electrodo estándar y el potencial de reducción estándar es que el potencial de electrodo estándar es la tendencia de un electrodo a perder o ganar electrones, mientras que el potencial de reducción estándar es la tendencia de una especie química dada a reducirse.
Referencia:
1. Helmenstine, Anne Marie. "Definición potencial de reducción estándar."Thinkco, agosto. 28, 2020.
Imagen de cortesía:
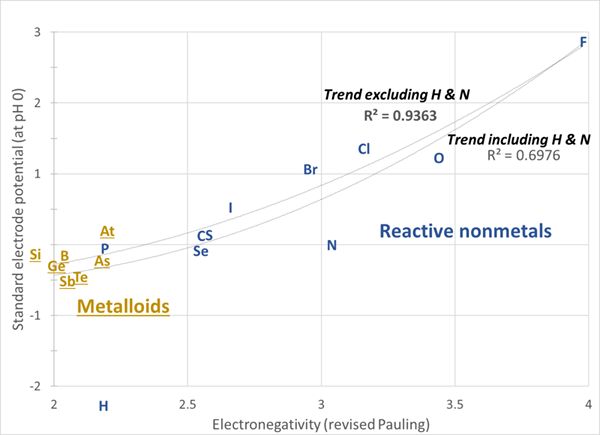
1. "EN & SEP de Elementsf no metálico" por SANDBH (versión original de abril de 2018); YBG (Versiones de junio de 2018) - Trabajo propio (CC BY -SA 4.0) a través de Commons Wikimedia


