¿Cuál es la diferencia entre el punto triple y el punto eutéctico?
El Diferencia clave entre el punto triple y el punto eutéctico es que en el punto triple, existen tres fases de una sustancia en equilibrio, mientras que en el punto eutéctico, una mezcla eutéctica particular se congela o se derrite.
Cambiar la temperatura y la presión de un sistema químico puede cambiar el estado físico o la fase de ese sistema porque los componentes en ese sistema tienen puntos particulares de fusión y ebullición en los que los cambios de fase tienen lugar entre las fases sólidas, líquidas y de gas.
CONTENIDO
1. Descripción general y diferencia de claves
2. ¿Qué es triple punto?
3. ¿Qué es el punto eutéctico?
4. Punto triple vs diagrama de punto eutéctico
5. Resumen -punto triple vs eutéctico
¿Qué es triple punto??
El punto triple es la temperatura y la presión a la que las fases sólidas, líquidas y de vapor de una sustancia particular coexisten en equilibrio. Describe un estado termodinámico específico de la materia. A veces, el punto triple puede involucrar más de una fase sólida cuando existen polimorfos de la sustancia. En un diagrama de fase, el punto triple es el punto en el que las tres líneas límite se encuentran entre sí.
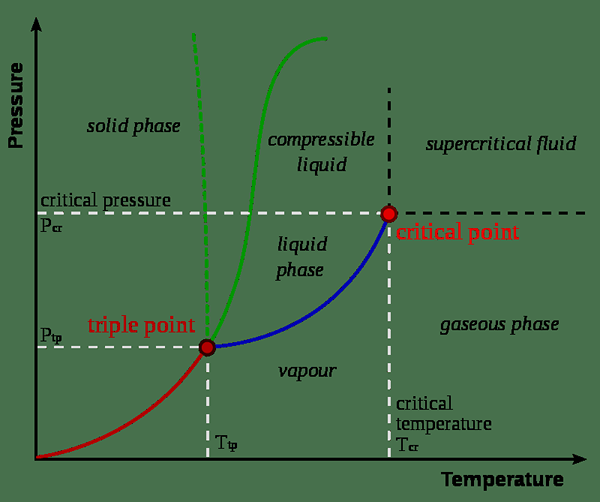
Figura 01: punto triple
¿Qué es el punto eutéctico??
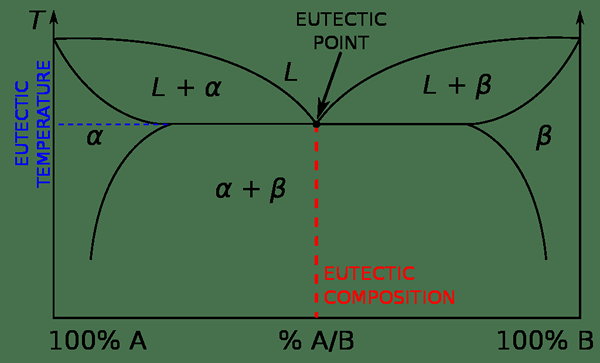
El punto eutéctico es la temperatura y la presión a la que una cierta mezcla líquida se transforma en dos fases sólidas al mismo tiempo al enfriar el líquido. Un sistema eutéctico es una mezcla homogénea de sustancias que pueden derretirse o solidificarse a una temperatura que es más baja que el punto de fusión de los componentes en esa mezcla. Además, el término temperatura eutéctica describe la temperatura de fusión más baja posible para todas las relaciones de mezcla posibles que están involucradas en la formación de la mezcla.

Figura 02: punto eutéctico
Al calentar una mezcla eutéctica, la red de un componente en la mezcla se derretirá primero a la temperatura eutéctica. Sin embargo, al enfriar el sistema eutéctico, cada componente en la mezcla tiende a solidificarse, formando la red de ese componente a una temperatura distinta. La solidificación ocurre hasta que todos los materiales se conviertan en sólidos. En general, un sistema eutéctico contiene dos componentes: por lo tanto, a temperatura eutéctica, el líquido se transforma en dos fases sólidas al mismo tiempo y a la misma temperatura. Por lo tanto, podemos nombrar este tipo de reacción como una reacción trifásica. Este es un tipo específico de reacción de fase; Por ejemplo, un líquido se solidifica, formando redes sólidas alfa y beta. Aquí, la fase líquida y la fase sólida están en equilibrio entre sí, un equilibrio térmico.
¿Cuál es la diferencia entre el punto triple y el punto eutéctico??
El punto triple es la temperatura y la presión a la que las fases sólidas, líquidas y de vapor de una sustancia particular coexisten en equilibrio. El término punto eutéctico es la temperatura y la presión a la que una cierta mezcla líquida se transforma en dos fases sólidas al mismo tiempo al enfriar el líquido. La diferencia clave entre el punto triple y el punto eutéctico es que en el punto triple, existen tres fases de una sustancia en equilibrio, mientras que en el punto eutéctico, una mezcla eutéctica particular se congela o se derrite. En otras palabras, en el punto triple, tres fases coexisten a las mismas condiciones de temperatura y presión, mientras que en el punto eutéctico, un líquido se convierte en dos fases sólidas a la misma temperatura y condiciones de presión.
La siguiente infografía enumera las diferencias entre el punto triple y el punto eutéctico en forma tabular para la comparación de lado a lado
Resumen -punto triple vs eutéctico
En resumen, el punto triple es la temperatura y la presión a la que las fases sólidas, líquidas y de vapor de una sustancia particular coexisten en equilibrio, mientras que el punto eutéctico es la temperatura y la presión a la que una cierta mezcla de líquido se transforma en dos fases sólidas Al mismo tiempo al enfriar el líquido. La diferencia clave entre el punto triple y el punto eutéctico es que en el punto triple, existen tres fases de una sustancia en equilibrio, mientras que en el punto eutéctico, una mezcla eutéctica particular se congela o se derrite.
Referencia:
1. Connor, Nick. "¿Cuál es el punto triple de agua? Definición." Ingenieria termal, 3 de junio de 2019.
Imagen de cortesía:
1. "Phase-DiaG2" de Matthieumarechal (CC BY-SA 3.0) a través de Commons Wikimedia
2. "Diagrama de fase del sistema eutéctico" de Etektikum_new.SVG: *eutektikum.GIF: DR. Bérder Imederivative Work: Michbich (charla) Trabajo derivado: Wizard191 (charla) - eutektikum_new.SVG (CC BY-SA 3.0) a través de Commons Wikimedia


